业务咨询

![]() 发布时间:2023-04-14
发布时间:2023-04-14
![]() 环特生物
环特生物
![]() 浏览次数:7509
浏览次数:7509

编者按:目前,类器官研究往往聚焦于肿瘤以及胃肠道相关研究,在药物性肝损伤(DILI)方面的研究仍在少数,那么最近有没有关于类器官用于DILI研究的前沿突破呢?
今天,我们特别关注一项于2023年2月1日发表在《Journal of Hepatology》的最新研究——A human liver organoid screening platform for DILI risk prediction,该研究利用iPSC(人诱导多能干细胞)诱导出肝类器官,再利用其搭建了两个平台用于DILI风险预测,为药物研发及个性化风险预测提供了新平台。
一、研究背景
药物性肝损伤(DILI)是急慢性肝病的一种罕见但重要的病因[1,2]。据估计,22%的临床试验失败和32%的药物召回,是肝毒性引起的[3,4]。而目前发现的许多DILI病例在很大程度上独立于药物的使用剂量和持续时间,并且仅有一小部分接受治疗的患者会出现DILI,并且原因尚不明确,因此给预测带来了很大的障碍。
为了应对这一挑战,本研究利用iPSC(人诱导多能干细胞)诱导的人肝类器官在体外重现DILI,并将肝类器官用于高通量筛选和器官芯片,开发了一个包括生物标志物/分析物检测、高内涵成像表型分析和单细胞RNA测序的整合多组学平台,为DILI的解析提供了一个全面的平台。
二、主要研究结果
1. 将肝类器官用于基于384孔板的高内涵筛选和药物聚类
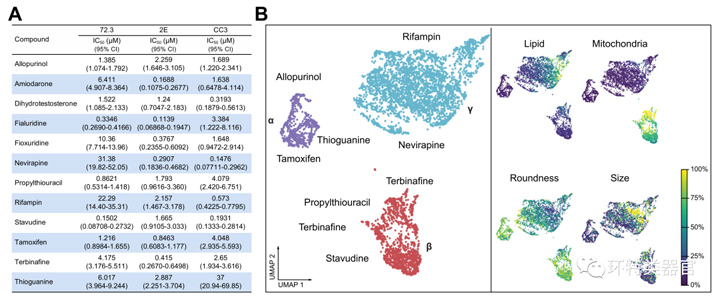
原文图1 将肝类器官用于基于384孔板的高内涵筛选和药物聚类
本研究利用三株iPSC(人诱导多能干细胞)细胞系(72.3、2E、CC3)诱导出三个来源的肝类器官,鉴定后发现这些肝类器官中肝细胞约占70%、肝星状细胞约占25%、库普弗细胞约占0.15%,与正常的肝脏较为类似。然后研究人员将肝类器官铺入384孔板中,用12种DILI相关药物处理后得到了一系列的IC50值,其中一些药物的IC50已低于血药浓度,这一体外实验提示一些受测药物有着强大的肝毒性。
该研究团队又利用CellProfiler 4.2.0对药物测试的肝类器官进行成像分析,再通过UAMP进行降维和聚类分析后发现,别嘌醇、他莫昔芬和硫鸟嘌呤处理后的细胞主要聚类于α簇,丙基硫氧嘧啶、核苷酸/核苷类似物处理后的细胞以及少量司他夫定、硫鸟嘌呤处理后的细胞聚类于β簇,而奈韦拉平和利福平处理后的细胞主要聚类于γ簇,说明这些药物虽然都会引起DILI,但其中的潜在机制可能存在差异。
2. 利用iPSC诱导的肝类器官构建肝器官芯片
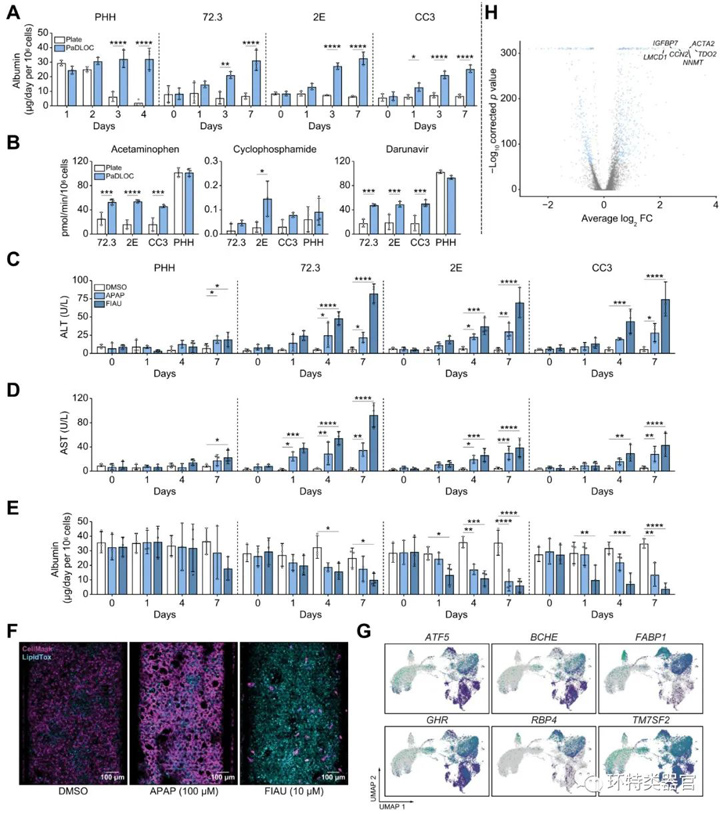
原文图2 构建基于肝类器官的肝器官芯片
研究人员将肝类器官消化成单细胞后,铺入Emulate的双通道芯片上,配合微流控技术,获得了一个肝器官芯片。就代谢特征而言,与培养于孔板中的肝类器官相比,肝器官芯片产生的白蛋白以及在代谢醋氨酚、环磷酰胺和地瑞那韦时产生的细胞色素P450也更多。而在基因特征层面,研究人员对肝器官芯片进行单细胞转录组测序后发现,肝器官芯片中增殖基因的表达较高,如TGFBI和CCN2。
表征了肝器官芯片的特点后,研究人员将其用于DILI的风险预测。目前在临床上,DILI的血清生物标志物包括谷丙转氨酶(ALT)和谷草转氨酶(AST)的升高以及白蛋白生成的减少[5]。用醋氨酚和非阿尿苷处理肝器官芯片后,ALT和AST都极显著升高,而白蛋白则显著减少,符合DILI的临床特征,而在相同处理下的原代人肝细胞系则没有如此剧烈的变化,说明肝器官芯片这一模型在DILI的预测方面优于原代人肝细胞系。
此外,研究人员还想了解肝器官芯片这一模型能否模拟体内药物毒性的内在机制。报道,醋氨酚可引起肝坏死[6],而非阿尿苷可引起脂质沉积毒害线粒体[7]。对肝器官芯片的细胞膜及脂质染色,也证实了这一点,说明肝器官芯片不仅能模拟体内的DILI,还能反映药物的毒理机制。
3. 替诺福韦和伊那吉韦联合用药的肝毒性建模
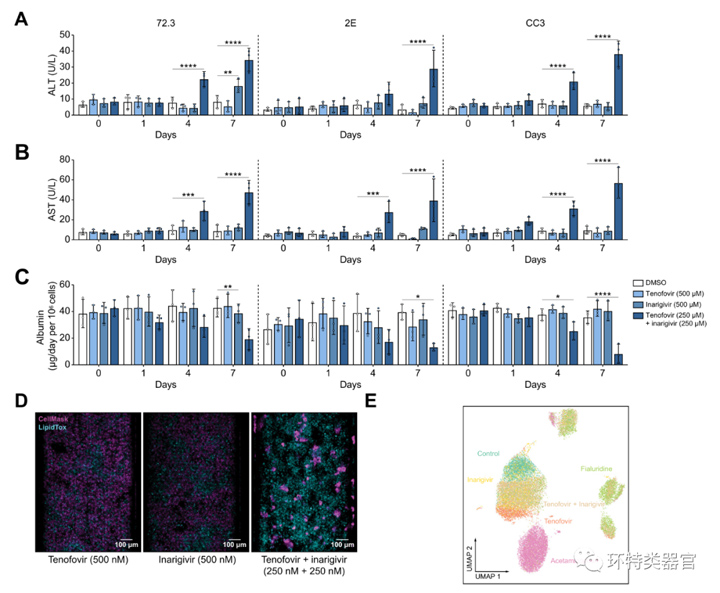
原文图3已知致DILI药物组合(替诺福韦+伊那吉韦)的评估
将肝类器官铺入384孔板中,用替诺福韦、伊那吉韦以及替诺福韦+伊那吉韦处理,结果显示,单药处理对肝类器官的活性几乎没有影响,而双药联用几乎杀死了所有肝类器官(IC50 = 56.9 μM)。
并且,将这三种用药方案用于肝器官芯片上,ALT、AST升高以及白蛋白的减少也与384孔板的结果保持一致。而对肝器官芯片的细胞膜及脂质染色揭示,替诺福韦+伊那吉韦联合用药的染色结果与非阿尿苷用药后的染色结果相似,这说明替诺福韦+伊那吉韦联合用药的毒理机制可能与非阿尿苷相似。并且细胞聚类分析也发现,替诺福韦+伊那吉韦联合用药与非阿尿苷处理后的细胞聚集在一类中。
4. 用药处理后的肝器官芯片的单细胞转录组分析
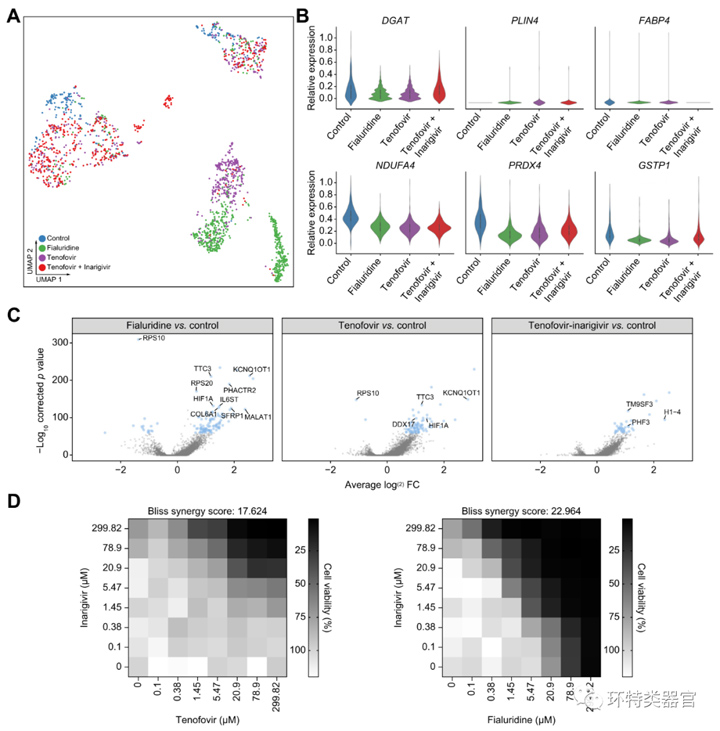
原文图4 用药处理后的肝器官芯片的单细胞转录组
为了弄清楚这些药物引起肝毒性的内在机制,研究人员对替诺福韦、替诺福韦+伊那吉韦、醋氨酚、非阿尿苷以及相应溶剂处理的肝器官芯片进行了单细胞转录组测序。结果显示,替诺福韦单药处理与非阿尿苷处理后的细胞最为相似,这两种药处理后的细胞中,KCNQ10T1基因(其上调被证明可以减轻DILI)表达都增多,并且脂肪酸、甘油三酯和脂质储存标志物的表达均呈现出同一特征。此外,这四种药物处理均会引起PLIN4基因(有助于脂滴在肝脏中的积累)表达的升高、NDUFA4和PRDX4基因(氧化应激的标志物)表达的减少。
因为在单细胞转录组的层面而言,替诺福韦单药处理与非阿尿苷的效果极为相似,因此研究人员推测非阿尿苷+伊那吉韦很可能会引起与替诺福韦+伊那吉韦类似的肝毒性,将非阿尿苷+伊那吉韦处理384孔板中的肝类器官后,果然不出所料的获得了相似的结果。因此,对联合用药的新组合进行了DILI的风险预测。
三、编者点评
1. 多年来,对于DILI的研究较多,但利用iPSC诱导的肝类器官进行的DILI的研究仍仅个位数,此外,本文还运用了微流控的器官芯片技术,构建肝器官芯片进行研究,因此本文在模型的运用方面有着较大的创新性;
2. 本文短小精悍,仅4个主要的Figure,推荐感兴趣的读者阅览;
3. 然而,本文仅对已知肝毒性的药物进行了验证性评估,没有利用如此优良的模型进行大规模的药物毒性筛查,在临床指导意义方面略有欠缺。
作为斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”四位一体的综合技术服务体系,开展科研及研发服务、智慧实验室建设和精准医疗三大业务。目前,环特类器官平台正在构建iPSC诱导的肝、肾类器官,用于药物毒理学评估,在下半年将推出药物毒性检测服务,敬请期待!
参考资料:
[1] Fontana RJ, Watkins PB, Bonkovsky HL, Chalasani N, Davern T, Serrano J, et al. Drug-Induced Liver Injury Network (DILIN) prospective study: rationale, design and conduct. Drug Saf 2009;32:55–68.
[2] Fontana RJ, Seeff LB, Andrade RJ, Björnsson E, Day CP, Serrano J, et al. Standardization of nomenclature and causality assessment in drug-induced liver injury: summary of a clinical research workshop. Hepatology 2010;52:730–742.
[3] Bakke OM, Manocchia M, de Abajo F, Kaitin KI, Lasagna L. Drug safety discontinuations in the United Kingdom, the United States, and Spain from 1974 through 1993: a regulatory perspective. Clin Pharmacol Ther 1995;58:108–117.
[4] Watkins PB. Drug safety sciences and the bottleneck in drug development. Clin Pharmacol Ther 2011;89:788–790.
[5] European Association for the Study of the Liver. Electronic address: easloffice@easloffice.eu, Clinical Practice Guideline Panel: Chair:, Panel members, EASL Governing Board representative: EASL Clinical Practice Guidelines: Drug-induced liver injury. J Hepatol 2019;70:1222–1261.
[6] Hinson JA, Roberts DW, James LP. Mechanisms of acetaminophen-induced iver necrosis. Handb Exp Pharmacol 2010:369–405.
[7] Kleiner DE. Drug-induced liver injury: The hepatic pathologist’s approach. astroenterol Clin North Am 2017;46:273–296.