业务咨询
![]() 发布时间:2024-03-20
发布时间:2024-03-20
![]() 环特生物
环特生物
![]() 浏览次数:6131
浏览次数:6131
为了更好地适应保健食品功能评价的需求,国家市场监督管理总局于2023年8月28日发布了《保健食品新功能及产品技术评价实施细则(试行)》(2023年第37号公告)。该细则明确了保健食品新功能的监管决策路径,并要求在上市后对新功能保健食品进行评价。这项细则的发布意味着国家对于保健食品新功能及其评价方法的认可和规范化。
针对保健食品新规,我们进行了保健食品新规系列解读↓↓,今天我们就来聊一聊保健食品研发与审评过程中的真实世界研究。
一、 真实世界研究(Real world study,RWS)
真实世界研究(Real world study,RWS)是指针对预设的临床问题,在真实世界环境下收集与研究对象健康有关的数据(Real world data,RWD)或基于这些数据衍生的汇总数据,通过分析,获得药物的使用情况及潜在获益-风险的临床证据(Real world evidence,RWE)的研究过程。简言之,RWS是将RWD转化为RWE的关键手段和桥梁。
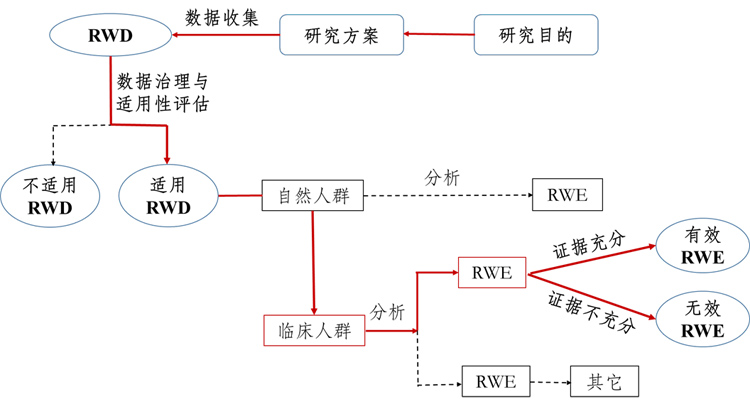
图1:支持药物监管决策的真实世界研究路径(实线所示)
二、保健食品RWS研究具有特殊性
在药品和医疗器械领域,RWS不断受到重视,RWE也被不断引入到监管决策的证据链收集体系。为指导真实世界证据用于支持药物研发和审评等有关工作,国家药监局也相继发布了《真实世界证据支持药物研发与审评的指导原则(试行)》、《用于产生真实世界证据的真实世界数据指导原则(试行)》等一批真实世界研究相关指导原则,为真实世界证据支持药物研发与审评奠定了基础。
相较于药品,保健食品没有临床医生的指导,完全依靠自主选择,因此保健食品上市前的研究结论外推于人群使用实际时会面临更大的挑战,不仅试验人群更不能充分代表目标人群,且所采用的标准干预与实际应用差别更大,同时由于保健食品无食用期限,上市前有限的样本量和较短的随访时间对食用人群不良感受的探测更加不足,而RWS可在相当程度上对此进行弥补,因此保健食品上市后技术评价更应重视RWS。
目前在国家层面尚未发布专门针对保健食品真实世界研究的指导原则,因此可以借鉴《真实世界证据支持药物研发与审评的指导原则(试行)》来指导保健食品的真实世界研究。
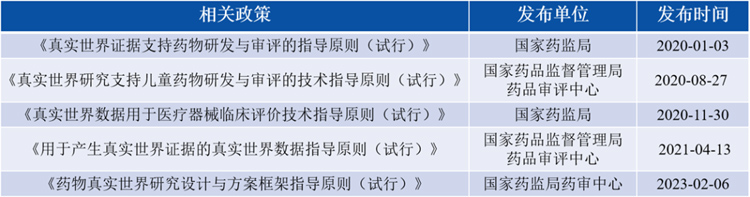
图2:国家发布的真实世界研究相关指导原则
三、RCT和RWS研究的差异
当前,保健食品的审批申报主要依赖随机对照试验(Randomized Controlled Trial,RCT)等方法进行功能验证,包括动物实验和小样本人群试食试验。然而,传统的RCT试验方法在验证保健食品的功能作用方面存在一些局限性。这些方法需要人为干预、纳排标准严苛、样本量有限且随访时间较短,因此难以完全评估保健食品的功能。
在保健食品的研发过程中,RCT属于药物面市前研究,关注的是效力研究,即保健食品或干预措施能否在理想、严格控制的环境下产生预期的效果,着重于干预措施的内部有效性,即期望获得高质量的研究证据。
而RWS属于保健食品面市后研究,关注效果研究,即评价药物在真实临床环境下的治疗效果,重在外部有效性。简单来说就是,RCT需要证明药物安全有效,而真实世界的证据来得到保健食品在实际使用中是安全的,也是有效的,并且得到更好和更适合的使用场景。
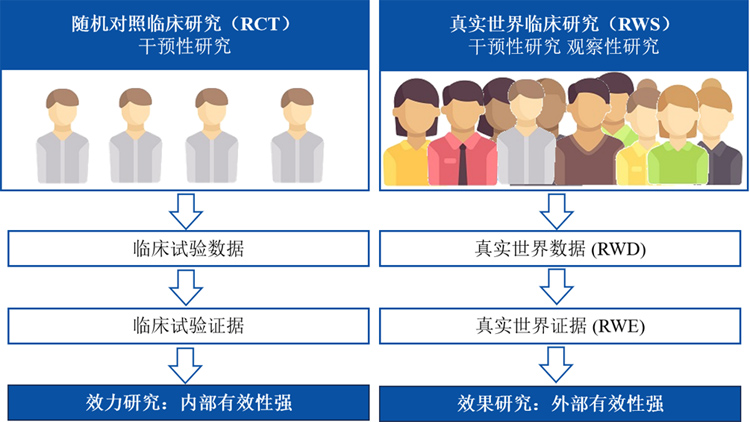
图3:RCT和RWS研究的区别
四、保健食品RWS的研究价值
RWS在支持药物监管决策方面已经得到应用。类似地,保健食品的RWS应用可涵盖上市前临床研发以及上市后再评价等多个环节。
开展保健食品的RWS可作为保健食品功能人体试食试验的补充,用于评估长期食用的功能有效性和安全性,提供更加科学的使用方式(包括食用剂量和周期)、更广泛的获益人群以及明确的禁用人群等信息。
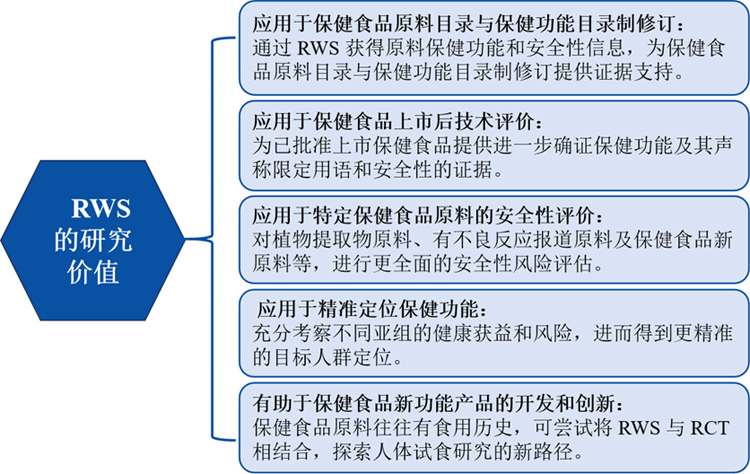
图4:保健食品RWS的研究价值
五、 保健食品RWS的研究设计和常见类型
RWS的开展须从营养健康问题的确定、现有数据情况的评估切入(采用既往回顾性数据或是前瞻性采集数据,进一步到研究设计的选择以及统计分析方法的确定、数据的管理、统计分析、结果解读和评价、以及根据需求判断是否加入事后分析等步骤。由于真实世界研究可能存在一些内在的偏倚,这些偏倚可能限制了真实世界数据在因果关系上的推理和解读。相较于 RCT,RWS的统计分析中需要特别注意对混杂效应的控制或调整,以避免得出有偏倚的效应估计。
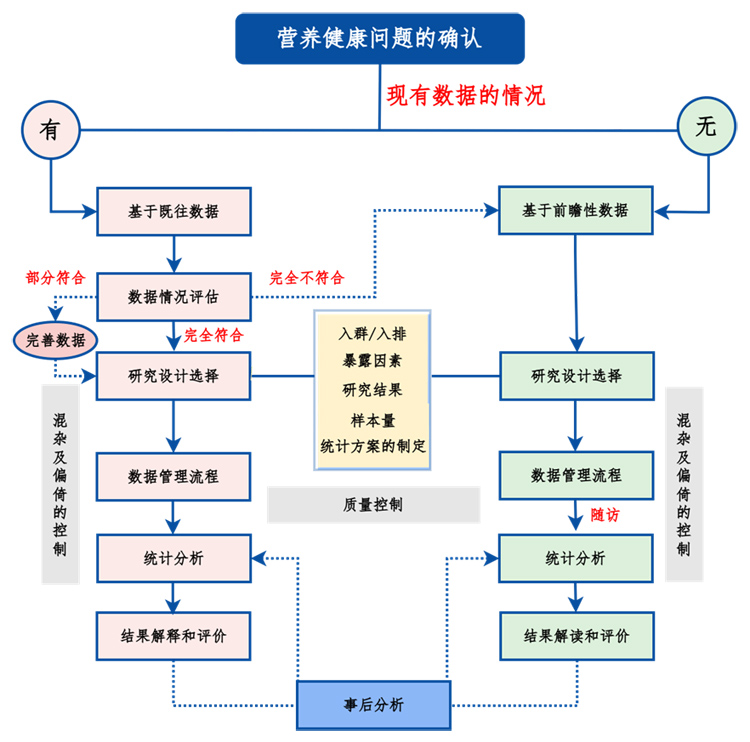
图5:RWS的研究设计
RWS的研究类型有多种,大致分为非干预性(观察性)研究和干预性研究。单臂研究设计是一种特殊的设计形式,其研究组可以是干预性的,也可以是观察性的,其外部对照通常基于RWD而设定。干预性研究主要是实效性临床试验。非干预性研究类型主要包括队列研究、病例对照研究、横断面研究等,根据需要根据不同的研究目的,选择适当的试验设计。
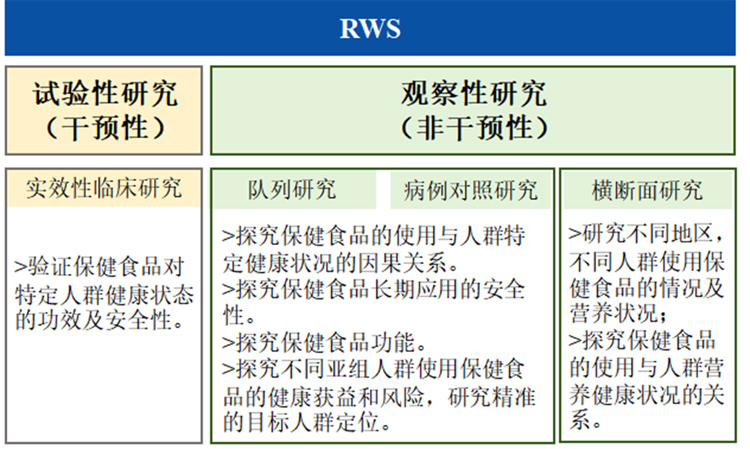
图6:RWS的研究分类
六、总结
在国家政策层面,推行RWS不仅有助于提升保健食品原料目录与保健功能目录制修订速度,还可为新产品研发和上市后技术评价提供证据。随着保健食品领域对真实世界研究的重视,未来也有望出台相应的指导原则与政策,以规范和指导保健食品的真实世界研究,为保健食品的研发、监管和推广提供更加明确的方向和依据。
对于保健食品而言,RWS能够在保健食品的真实食用环境中进行,产生的RWE能够更有力地证明保健食品干预措施的安全性和保健功能。推行RWS可以为保健食品特定原料的安全性和精准定位保健功能提供证据支持,并最大限度地保留占保健食品总数70%以上的中药组方保健食品的养生保健理论特征。通过全面认识和理解 RWD和RWE,并依托现代化电子数据平台、大数据、区块链等先进技术和理念,有助于突破保健食品的研发瓶颈,推动保健食品产业发展,为健康中国做出更大贡献。
环特生物与多家具备注册或备案验证评价工作法定资质机构开展深度合作,可为各类保健功能食品的申报提供丰富的人体试食试验方案。同时,还提供集斑马鱼生物技术、哺乳动物实验平台、基因编辑技术等多维生物技术为一体的全方位、一体化的安全性和功效研究体系,为健康美丽产业探索多元化CRO与科研服务新路径,助力保健食品创新研发与应用!
【技术咨询】17364531293(微信同号)
参考文献:
[1] 王进博,陈广耀.真实世界研究对保健食品研发与审评的价值[J].中国循证医学杂志, 2020, 20(10):4.
[2]《真实世界证据支持药物研发与审评的指导原则(试行)》.
[3]《药物真实世界研究设计与方案框架指导原则(试行)》.


