业务咨询

![]() 发布时间:2025-06-03
发布时间:2025-06-03
![]() 环特生物
环特生物
![]() 浏览次数:2336
浏览次数:2336

编者按
非酒精性脂肪性肝病(NAFLD)是非酒精性脂肪性肝炎、肝纤维化、肝硬化以及潜在肝细胞癌的主要病因。野菊花(Chrysanthemum indicum)作为一种传统的食药同源植物,在中国已有超过2000年的应用史。然而,关于野菊花在非酒精性脂肪性肝病治疗中的作用很少被研究。
今天,我们分享由澳门大学中医研究所张庆文、林理根研究团队发表在J Adv Res.(IF=11.4)的一项最新研究成果。该研究旨在揭示野菊花治疗NAFLD的新型活性成分及其潜在机制的,结果表明:野菊花新型倍半萜类化合物通过减轻SIRT1介导的脂质积累和铁死亡来缓解肝脏脂肪变性,为进一步开发治疗NAFLD的候选药物提供了强大工具。
研究人员在基于MS/MS的分子网络指导下,从野菊花中分离得到27个新型二聚倍半萜类化合物——chryindicolides A-Z (1-26) 和 chrysanthemolide C (27),以及7个已知化合物。其中,化合物1-7为罕见的含氯愈创木内酯二聚体;Chryindicolide O (15) 能直接结合并激活去乙酰化酶Sirtuin 1 (SIRT1),从而在棕榈酸和油酸(P/O)诱导的AML12肝细胞中减少脂质新生、增强脂肪酸β-氧化并抑制铁死亡;Chryindicolide O也显著改善了高脂饮食喂养的斑马鱼肝脏脂肪变性。
文章题目
Dimeric guaianolide sesquiterpenoids from the flowers of Chrysanthemum indicum ameliorate hepatic steatosis through mitigating SIRT1-mediated lipid accumulation and ferroptosis
杂志:J Adv Res.(IF=11.4)
发表时间:2025年1月7日
作者:张庆文、林理根等
单位:澳门大学中医研究所等
01、研究亮点
• 从野菊花中靶向分离出 27种新型二聚倍半萜化合物——chryindicolides A-Z及chrysanthemolide C),其中化合物1-7为罕见的含氯愈创木内酯二聚体;
• Chryindicolide O可改善肝细胞和斑马鱼的肝脂肪变性,其作用机制明确;
• Chryindicolide O直接结合并激活去乙酰化酶Sirtuin 1(SIRT1);
• Chryindicolide O抑制脂质新生(DNL),增强脂肪酸β-氧化(FAO);
• Chryindicolide O抑制SIRT1介导的铁死亡。
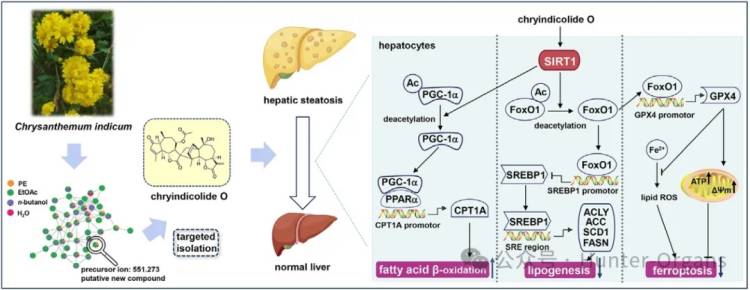
摘要
02、研究背景
非酒精性脂肪性肝病(NAFLD) 是全球最常见的肝脏疾病,影响着全球约四分之一的人口。肝细胞中异位脂质的积累及其后续的脂毒性明显加速了NAFLD的进展。因此,减轻肝细胞内的脂质积累成为非酒精性脂肪性肝病治疗的一种可行策略。
肝脏脂质代谢的调控涉及脂质新生(de novo lipogenesis, DNL) 和脂肪酸β-氧化(fatty acid β-oxidation, FAO)等多个过程。DNL即利用膳食来源物质来生产内源性合成脂质。人体同位素标记研究表明,NAFLD患者的DNL比非酒精性脂肪性肝病患者的DNL对肝脏甘油三酯(TG)的积累高三倍。FAO是脂肪酸降解的主要途径,线粒体中FAO的损伤不仅导致肝细胞内脂质积累,还会通过活性氧(ROS)释放和氧化损伤引发炎症,从而加重NAFLD的发展。因此,减少DNL和增强FAO是减轻肝脏脂质积累的有效策略。
铁死亡(Ferroptosis)作为一种独特的细胞死亡形式,依赖于铁介导的芬顿反应(Fenton reaction),促进自由基和ROS的生成。铁过载和脂质过氧化通常被认为是铁死亡的主要特征。在NAFLD的初始阶段,肝脏铁水平和氧化应激显著升高,甚至比典型的NAFLD指标,如肝脏脂肪酸堆积、胰岛素抵抗等提前两周。另一项生物信息学研究也揭示了肝脏脂肪变性的进展与多个铁死亡相关基因,如酰基辅酶A合成酶长链家族成员3 (ACSL3)、脂肪酸去饱和酶2 (FADS2) 、醛酮还原酶家族1成员C1 (AKR1C1))。
多不饱和脂肪酸(PUFA) 通常被认为是脂质过氧化的主要底物,脂质过氧化导致长链PUFA(LCPUFA)的消耗,如ω-3和ω-6 LCPUFA。ω-3 LCPUFA的减少可能通过刺激肝脏DNL和抑制肝脏FAO来增强肝脏脂肪变性。此外,脂质ROS通过增加脂滴的形成来增强肝脏脂肪变性,而清除铁死亡相关的脂质过氧化物则有助于减少脂质积累。因此,抑制铁死亡有助于恢复肝细胞内的铁稳态,并抑制非酒精性脂肪性肝病的发展。减少脂质积累和抑制铁死亡是非酒精性脂肪性肝病相关症状治疗的有效途径。
越来越多的证据表明,天然产物,尤其是萜类化合物,能够有效缓解NAFLD的相关症状,是治疗非酒精性脂肪性肝病的有潜力的候选药物。野菊花作为一种药食同源草本植物,在中国、日本和韩国等地已有超过2000年的广泛应用史。作为一种传统中药,野菊花具有清热解毒、泻火、平肝等多种特性。现代药理学研究已证明其具有抗炎、抗癌、抗氧化、保肝和抗菌作用等广泛的生物活性。此外,野菊花也是一种受欢迎的营养健康补充剂,因其对治疗溃疡、痈疮、眼睛肿胀、头痛和头晕有效,而被用于汤、饮料和茶中。先前的研究发现,野菊花的乙醇和乙酸乙酯提取物可减轻高脂饮食喂养的小鼠肝脏脂肪变性。然而,野菊花在治疗非酒精性脂肪性肝病中的有效成分及其潜在机制尚不清楚。
倍半萜类及其聚合物因其结构复杂性和多样的生物活性,如抗癌、抗炎、抗肥胖、抗糖尿病、抗病毒和抗疟活性等而引起了越来越多研究者的兴趣。最近的研究强调了倍半萜类二聚体在菊科(Asteraceae)和金粟兰科(Chloranthaceae)中普遍存在,其中愈创木烷型(guaiane-type)倍半萜类二聚体主要分布在菊科。目前,愈创木内酯二聚体主要是从蒿属(Artemisia)植物中鉴定出来,其中仅有大约15 种愈创木内酯二聚体是从野菊花(C. indicum)中分离出的。
全球天然产物分子网络(GNPS)已成为一种强大的工具,能够基于样品的UPLC-MS/MS谱图,从多个样品中生成分子网络。其利用结构相关分子在MS/MS 谱图中的相似性创建而成,有助于阐明已知化合物及发现新的类似物。因此,本研究采用分子网络引导策略对野菊花进行了全面的植物化学研究,并鉴定了27种新型倍半萜类化合物,还评估了这些分离得到的化合物在治疗肝脂肪变性中的作用及其潜在机制。
03、研究结果
1. 基于MS/MS的分子网络构建
研究人员将野菊花95%的EtOH提取物分为PE、EtOAc、n-butanol和H2O组分,扫描获得每个组分的UPLC-MS/MS谱图,将其导入GNPS生成分子网络。基于MS/MS的分子网络指导下,从野菊花中分离得到27个新型二聚倍半萜类化合物——chryindicolides A-Z (1-26) 和 chrysanthemolide C (27)(图1);并通过光谱解析了化合物1–27的结构,鉴定了化合物1-7为罕见的含氯愈创木内酯二聚体,确定了愈创木内酯倍半萜类化合物的两种二聚化模式。
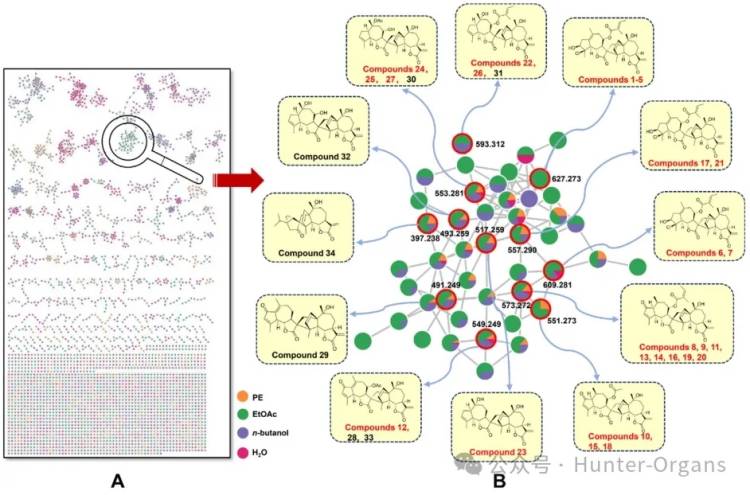
图1
2. Chryindicolide O抑制脂质新生(DNL),增强脂肪酸β-氧化(FAO)
P/O 溶液诱导的肝细胞脂质积累模型常被用于NAFLD体外研究。研究人员采用MTT法评估化合物对AML12肝细胞的细胞毒性,确定最大安全浓度后,对分离得到的化合物在P/O诱导的AML12细胞中进行了降脂作用研究。尼罗红染色结果显示,20种化合物在最大安全浓度下表现出降脂作用,其中,化合物10、13、15、23、29和30改善脂肪变性作用显著;其余14种化合物在最大安全浓度下,抑制率均小于50 %。
作为最有效的化合物,Chryindicolide O(15)被选作研究对象,尼罗红和BODIPY染色结果表明,化合物15(2.5、5、10 μM)在P/O诱导的AML12细胞中,剂量依赖性地降低了脂质积累,且15以浓度依赖的方式降低了P/O诱导的AML12细胞中甘油三酯(TG)、总胆固醇(T-CHO)和非酯化脂肪酸(NEFA)的含量。肝脏DNL在肝脏脂肪变性中起着重要作用。固醇调节元件结合蛋白(SREBPs)是调控DNL通路相关基因的关键转录因子,在NAFLD的发生发展中发挥着重要作用。结果显示,15降低了ACLY、ACC、FASN和SCD1的蛋白水平。化合物15能够有效促进FoxO1的去乙酰化,抑制SREBP1的蛋白表达和核转位,从而降低DNL。
随后,研究人员检测了化合物15对FAO相关蛋白表达的影响,P/O诱导降低了CPT1A的表达,而化合物15明显逆转了这一变化,依赖性地促进了PPARa的总蛋白和核蛋白水平。P/O诱导降低了AML12细胞中PGC-1q的蛋白表达,促进了PGC-1q的乙酰化,表明PGC-1q活性受损。而用15处理后,PGC-1G的蛋白表达明显增加,乙酰化水平降低。免疫共沉淀分析表明,化合物15处理后PPARα沉淀的PGC-1α量增加,表明15促进了PGC-1α与PPARG的结合。综上,化合物15促进了PGC-1q的表达和去乙酰化,从而促进其与PPARG的结合,并增强其转录效应以增加CPT1A的表达,导致FAO增加、脂质积累减少。
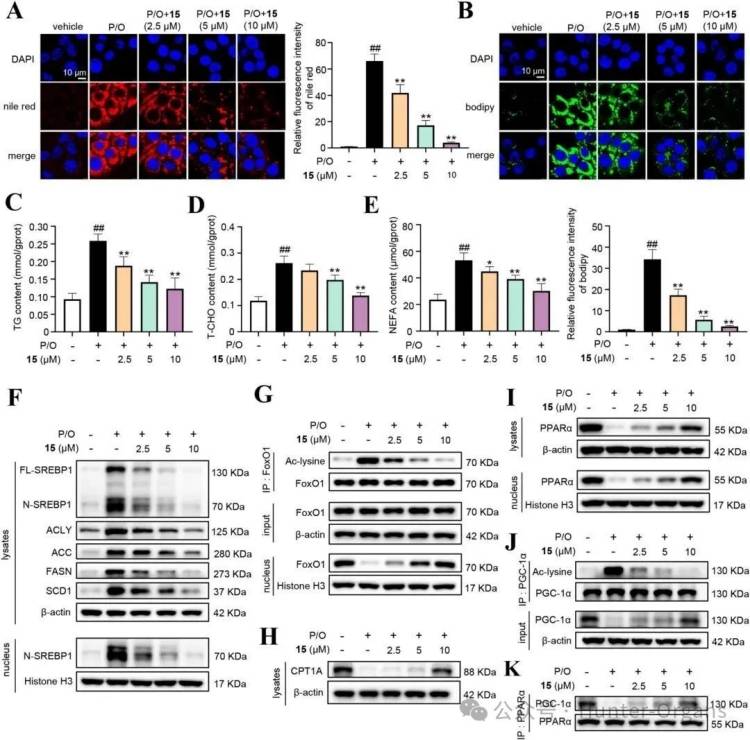
图2
3. Chryindicolide O直接结合并激活SIRT1
Sirtuin 1(SIRT 1)是一组III型的蛋白脱乙酰酶,被认为是新的参与细胞衰老和炎症调节的抗衰老蛋白,通过去乙酰化一系列底物,在对抗NAFLD的进展中起着至关重要的作用。P/O处理降低了SIRT1的蛋白表达,而化合物15处理逆转了这种变化。DARTS证实了化合物15对链霉蛋白酶诱导的SIRT1蛋白降解的抑制作用,且化合物15与SIRT1直接结合。结果显示,与vehicle组相比,化合物15减弱了SIRT1的降解。分子对接结果表明,化合物15是SIRT1的潜在激活剂。总之,化合物15直接与SIRT1的SBD结合和激活SIRT1,并通过抑制泛素依赖性蛋白降解来促进SIRT1蛋白表达。
此外,通过尼罗红染色和BODIPY染色评估发现,EX-527处理使P/O诱导的 AML 12肝细胞脂质含量更高,并消除了15对脂质积累的抑制作用,E且X-527逆转了化合物15对甘油三酯(TG)、总胆固醇(T - CHO)和非酯化脂肪酸(NEFA)含量的降低作用。WB和免疫荧光图像结果显示,EX-527处理消除了15减少FoxO1乙酰化、增加FoxO1在细胞核内滞留的影响,并显著增加了SREBP1蛋白水平和细胞核内滞留。通过PGC-1α/PPARα/CPT1A 信号通路,发现EX-527几乎消除15增加CPT1A 蛋白表达的作用。这表明,化合物15通过直接结合和激活SIRT1来减少肝细胞中的脂质积累。
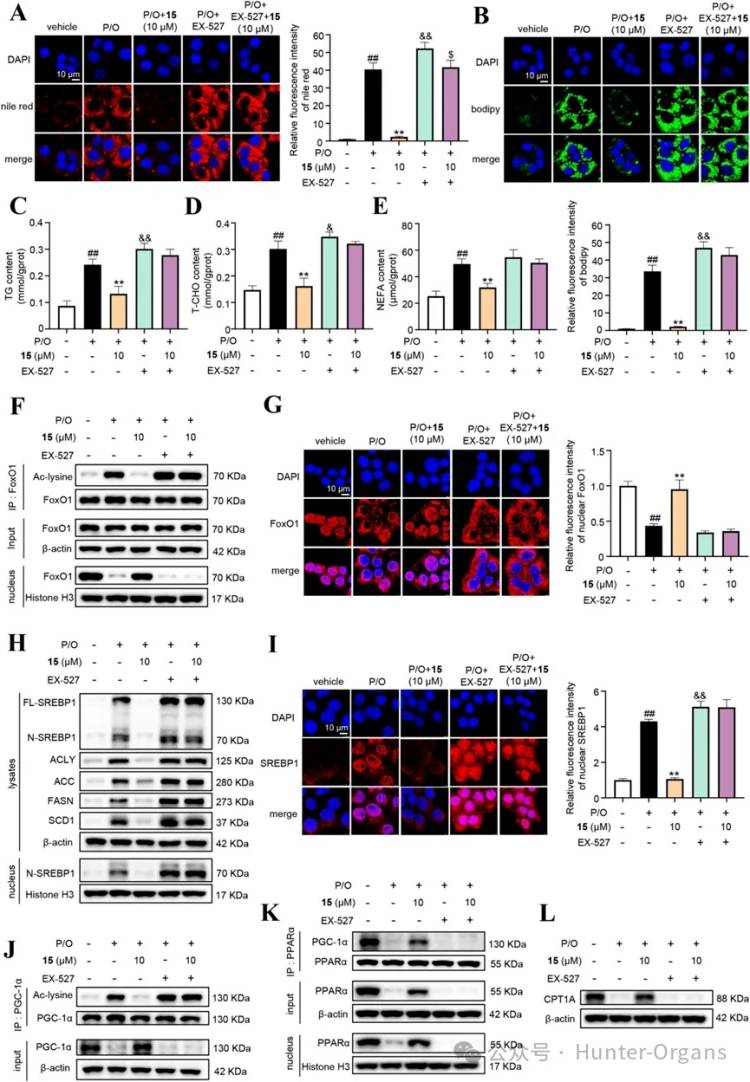
图3
4. Chryindicolide O抑制SIRT1介导的铁死亡
研究中,在P/O暴露的AML12细胞中,化合物15使GPX4蛋白水平呈浓度依赖性增加,并伴随FoxO1核转位增加。为进一步证明化合物15通过抑制铁死亡保护肝细胞,通过检测相关生化指标发现,P/O处理增加了细胞内铁死亡的显著特征脂质过氧化和ROS水平等,而化合物15明显减弱了这些变化,且呈剂量依赖性,表明化合物15抑制了铁死亡。EX-527处理还增加了P/O处理的肝细胞内的脂质过氧化和ROS水平灯,表明抑制SIRT1可能加重铁死亡。
P/O处理后,谷甘肽(GSH)水平和SOD活性呈下降趋势,而MDA水平升高,表明氧化还原系统受损;而在P/O诱导的AML12细胞中,化合物15处理导致GSH水平和SOD活性增加,而MDA降低,EX-527取消了这一作用。化合物15处理也降低了P/O处理的肝细胞中的线粒体ROS(mtROS),增加了P/O诱导的AML12细胞中的Fe²⁺含量、线粒体含量、ATP含量等。总之,在P/O处理的AML12细胞中,化合物15通过SIRT1降低脂质过氧化及Fe²⁺含量,并通过SIRT1改善线粒体含量和功能来缓解铁死亡。
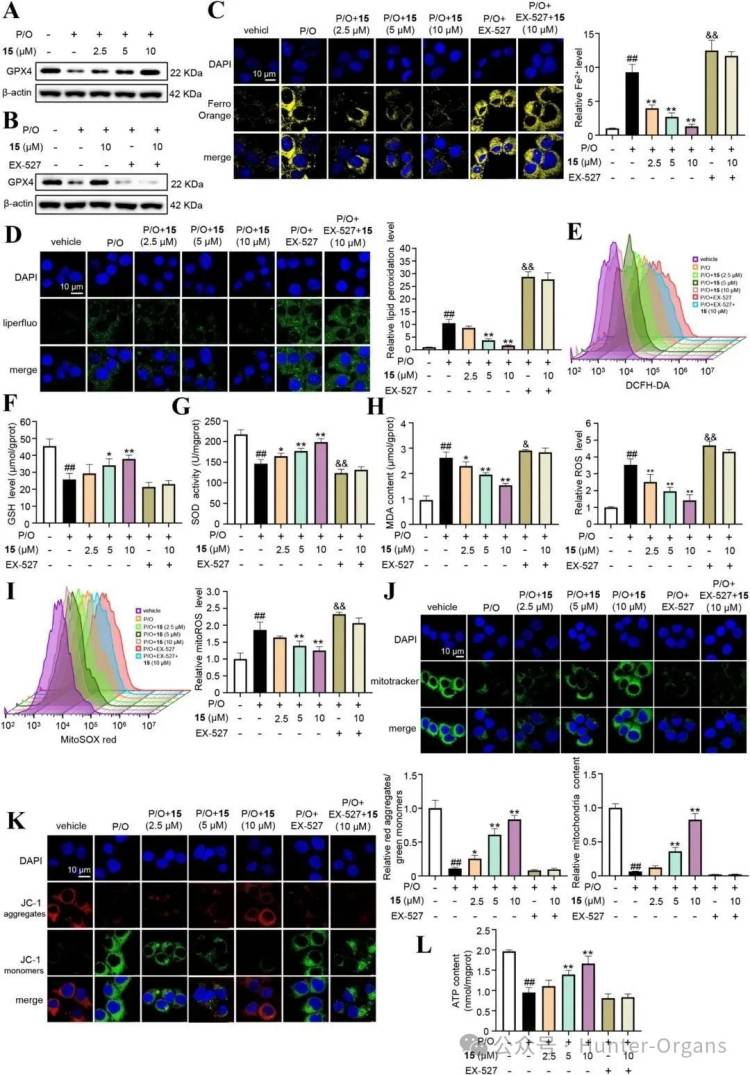
图4
5. Chryindicolide O可减轻高脂饲料喂养的斑马鱼肝脏脂肪变性
随后,研究人员构建了斑马鱼NAFLD模型,利用高脂饲料喂养的斑马鱼证实了化合物15对NAFLD的抑制作用。实验结果显示,斑马鱼体重显著降低,正常斑马鱼肝脏组织形态正常,有完整且排列紧密的肝细胞空泡,HFD组肝细胞空泡多、肝细胞变形且排列不规则,而化合物15处理后肝脏空泡更小、更少。
油红O染色表明化合物15处理后的斑马鱼肝脏脂滴减少,甘油三酯(TG)、总胆固醇(TCHO)、非酯化脂肪酸(NEFA)水平及谷丙转氨酶(ALT)、谷草转氨酶(AST)活性显著降低。且15处理后也降低了活性氧(ROS)和丙二醛(MDA)含量,增加了谷胱甘肽(GSH)水平和超氧化物歧化酶 2(SOD2)活性,这表明15对NAFLD的抑制作用,缓解了高脂饲料喂养的斑马鱼肝脏脂肪变性。
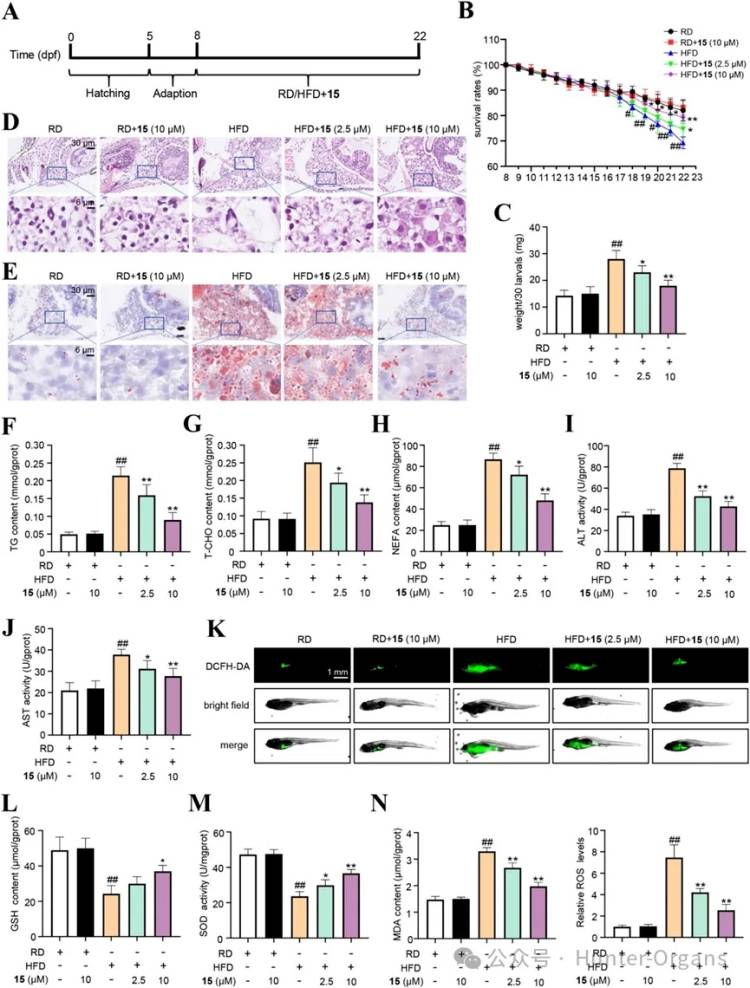
图5
04、编者点评
本研究首次揭示了野菊花倍半萜类化合物通过SIRT1双途径——脂代谢与铁死亡来改善脂肪肝,并阐明SIRT1-FoxO1/SREBP1与SIRT1-PGC-1α/PPARα/CPT1A通路串扰,及SIRT1-GPX4抗铁死亡新机制,为天然抗NAFLD候选药物提供了新来源,有望基于新化合物来治疗NAFLD提供新策略。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,胃癌、脑类器官、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!